Chemistry Tamil Medium - Online Test
குளிர்ந்த நீரில் கார்பன்டை ஆக்சைடு வாயுவின் கரைதிறனை எவ்வாறு அதிகரிக்கலாம்.
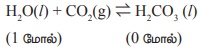
அழுத்த அதிகரிப்பு, முன்னோக்கு வினையை ஆதரிக்கும் .
ஒரு
நீர்மத்தில் வாயுவின் கரைதிறனானது அழுத்தத்தை அதிகரிக்கும் போது
அதிகரிக்கிறது.
350 K வெப்பநிலையில் நீரில், நைட்ரஜன் வாயுவின் கரைதிறனுக்கு ஹென்றி விதி மாறிலி மதிப்பு 8 × 104 atm. காற்றில் நைட்ரஜனின் மோல் பின்னம் 0.5 ஆகும். 350K வெப்பநிலை மற்றும் 4 atm அழுத்தத்தில் 10 மோல்கள் நீரில் கரையும் காற்றிலுள்ள நைட்ரஜனின் மோல் எண்ணிக்கை
KH = 8 × 104 ;
(Xn2) காற்றில் = 0.5
மொத்த
அழுத்தம் = 4 atm
நைட்ரஜனின் பகுதி
அழுத்தம் = மோல்
பின்னம் × மொத்த
அழுத்தம் = 0.5 × 4 = 2
(Pn2) = KH × கரைசலில் N2 ன் மோல் பின்னம்

2‒ பியுட்டைனலில் (2‒butynal) உள்ள சிக்மா (σ) மற்றும் பை (π) பிணைப்புகளின் எண்ணிக்கைக்கு இடையேயுள்ளவிகிதம்
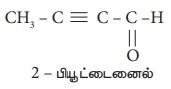
σ பிணைப்புகள் எண்ணிக்கை = 8[4C-H;,3C-C;1C-O]
π பிணைப்புகள் எண்ணிக்கை = 3[2C-C; 1C-O]
விகிதம் = 8/3
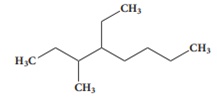 என்ற சேர்மத்தின் IUPAC பெயர்
என்ற சேர்மத்தின் IUPAC பெயர் இணைதிறன் மூன்று கொண்ட உலோகத் தனிமத்தின் சமான நிறை 9g.eq‒1 அதன் நீரற்ற ஆக்ஸைடின் மூலக்கூறு நிறை
இணைதிறன் மூன்று
கொண்ட
உலோகத்தினை M3+ என்க
சமான
நிறை
= உலோகத்தின் நிறை
/ சமான
காரணி
9g eq−1 = உலோகத்தின் நிறை / 3eq
உலோகத்தின் நிறை
= 27g
உருவாகும் ஆக்ஸைடு = M2O3 ;
ஆக்ஸைடின் நிறை
= (2 × 27) + (3 × 16)
= 102g
போர் அணுக்கொள்கையின் அடிப்படையில், ஹைட்ரஜன் அணுவில் பின்வரும் எந்தப் பரிமாற்றம் குறைவான ஆற்றலுடைய போட்டானைத் தரும்.
n = 6 to n = 5
E6 = −13.6 / 62;
E5 = −13.6 / 52
E6 – E5 =
(−13.6/62) − (−13.6/52)
= 0.166 eV atom−1
E5 – E4 =
(−13.6/52) − (−13.6/ 42)
= 0.306 ev atom−1
Hyper
Conjucation இவ்வாறும் அழைக்கப்படுகிறது
ஒரு தனிமத்தினுடைய அடுத்தடுத்த அயனியாக்கும் ஆற்றல் மதிப்புகள் கீழே கொடுக்கப்பட்டுள்ளன (kJ mol‒1)
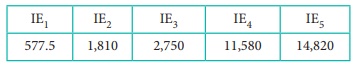
இத்தனிமானது
வேதிவினைக்கூறு விகிதத்தின் அடிப்படையில் அமையாத (non – stoichiometric) ஹைட்ரைடுகளை உருவாக்குபவை