Chemistry Tamil Medium - Online Test
50 mL 8.5
% AgNO3 கரைசலை 100 mL. 1.865% பொட்டாசியம் குளோரைடு கரைசலுடன் சேர்க்கும் போது கிடைக்கும் வீழ்படிவின் எடை என்ன?
AgNO3 + KCl → KNO3
+ AgCl
50 mL 8.5% கரைசல் ஆனது 4.25g AgNO3 −ஐக் கொண்டுள்ளது. 50 mL 8.5% AgNO3 கரைசலில் உள்ள
AgNO3 ன்
மோல்களின் எண்ணிக்கை = நிறை
/ மோலார்
நிறை
= 4.25/170 = 0.025 மோல்கள்
இதைப்போலவே, 100 mL 1.865% KCl கரைசலில் காணப்படும் KCl ன்
மோல்களின் எண்ணிக்கை = 1.865 / 74.5
= 0.025 மோல்கள்
எனவே
உருவாகும் AgCl ன்
மொத்த
அளவு
0.025 மோல்கள் (வேதி
வினைக்கூறு விகிதத்தின் அடிப்படையில்)
0.025 மோல்கள் AgCl ல்
காணப்படும் AgCl − ன் அளவு
= மோல்களின் எண்ணிக்கை × மோலார்
நிறை
= 0.025 × 143.5 = 3.59g
நிலை மற்றும் உந்தத்தின் நிச்சயமற்றத் தன்மை சமம் எனில், அதன் திசைவேகத்தின் குறைந்தபட்ச நிச்சயமற்றத் தன்மை

புரப்பைனை செஞ்சூட்டு நிலையில் உள்ள இரும்புக் குழாயின் வழியே செலுத்தும் போது பெறப்படும்
Na, Mg மற்றும் Si ஆகியவைகளின் முதல் அயனியாக்கும் ஆற்றல் முறையே 496, 737 மற்றும் 786 kJ mol‒1 ஆகும். Al‒ன் அயனியாக்கும் ஆற்றல் பின்வரும் எந்த மதிப்பிற்கு அருகில் இருக்கும்.
கனநீர் பயன்படுவது
பின்வருவனவற்றுள் கருக்கவர் பொருள் பதிலீட்டு வினையில் அதிக வினைபுரிவது எது?
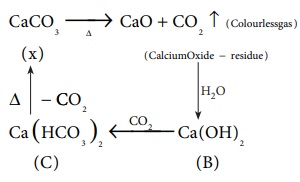
சேர்மம் (X) ஐ வெப்பப்படுத்தும்போது நிறமற்ற வாயுவையும், ஒரு வீழ்படிவையும் தருகிறது. அந்த வீழ்படிவை நீரில் கரைத்து சேர்மம் (B) பெறப்படுகிறது. சேர்மம் (B) ன் நீர்க்கரைசலில் அதிகளவு CO2 ஐ குமிழிகளாக செலுத்தும்போது சேர்மம் (C) உருவாகிறது. (C) ஐ வெப்பபடுத்தும்போது மீண்டும் (X)ஐத் தருகிறது. சேர்மம் (B) ஆனது
நல்லியல்பு பண்பிலிருந்து அதிக விலக்கம் அடையும் வாயு
அனைத்து வெப்பநிலைகளிலும், ஒரு தன்னிச்சையான வினைக்கு சரியான வெப்ப இயக்கவியல் நிபந்தனைகள்
SO2
மற்றும் O2 ஆகியவற்றிலிருந்து இரண்டு மோல்கள் SO3 உருவாகும் வினைக்கு சமநிலை மாறிலி K1 ஒரு மோல் SO3 சிதைவுற்று SO2 மற்றும் O2 ஆகியவற்றைத் தரும் வினையின் சமநிலை மாறிலி
2SO2(g) + O2(g) ⇌ 2SO3(g) ; K1
SO3(g) ⇌ SO2(g) + ½ O2(g) ; K2