Chemistry Tamil Medium - Online Test
நீரில் இட்ட நீற்றுச் சுண்ணாம்பின் தொங்கல் கரைசல் __________ என அறியப்படுகிறது?
நீற்றுச் சுண்ணாம்பு Ca(OH)2
தொங்கலானது சுண்ணாம்புப் பால்
(Milk of Lime) என்றழைக்கப்படுகிறது. மேலும்
தெளிவான கரைசல்
சுண்ணாம்பு நீர்
(Lime Water) என்றழைக்கப்படுகிறது.
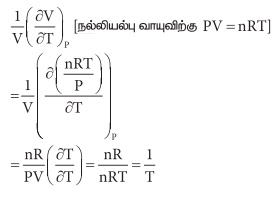
மாறாத அழுத்தத்தில் வெப்பநிலை மாற்றத்தால் ஏற்படும் கனஅளவு மாற்றம் கனஅளவின் ஒப்பீட்டு அதிகரிப்பு ஆகும். அதாவது α = (1 /
V) (∂V / ∂T )P. நல்லியல்பு வாயுக்களுக்கான α மதிப்பு
0°C வெப்பநிலை மற்றும் 1 atm அழுத்தத்தில் 15.68 L மீத்தேன் மற்றும் புரப்பேன் கலந்த வாயுக்கலவையை முற்றிலுமாக எரிக்க, அதே வெப்ப அழுத்தநிலையில் 32 L ஆக்ஸிஜன் தேவைப்படுகிறது, எனில் இந்த எரிதல் வினையில் வெளிப்படும் வெப்பத்தின் அளவு kJ அலகில்.
கொடுக்கப்பட்டவை
AHC(CH4) = ‒890
kJ mol−1
∆HC(C3H8)
= ‒2220 kJ mol−1
கலவையானது x லிட்டர் மீத்தேனையும் (15.68 − x) லிட்டர் புரப்பேனையும் கொண்டு
இருப்பதாகக் கருதுக.
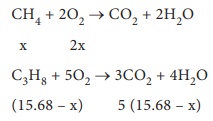
வினைப்பட்ட ஆக்சிஜனின் கனஅளவு
= 2x + 78.4 – 5x = 32 லிட்டர்
78.4 – 3x = 32
3x = 46.4 லிட்டர்
x = 15.47 லிட்டர்
கொடுக்கப்பட்டுள்ள கலவையானது 15.47 லிட்டர் மீத்தேனையும் 0.213 லிட்டர் புரப்பேனையும் கொண்டுள்ளது, எனவே

∆HC = −635.47 kJmol−1
ஒரு வேதிச் சமநிலையில், முன்னோக்கு வினையின் வினைவேக மாறிலி 2.5 × 102 மற்றும் சமநிலை மாறிலி 50 எனில் பின்னோக்கு வினையின் வினைவேக மாறிலி
Kf = 2.5 × 102;
K C = 50; K r = ?
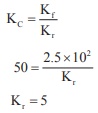
இரண்டு திரவங்கள் X மற்றும் Y ஆகியன கலக்கப்படும்போது வெதுவெதுப்பான கரைசலைத் தருகின்றன. அந்தக் கரைசலானது
ஒத்த இனக்கலப்பு, வடிவம் மற்றும் தனித்த எலக்ட்ரான் இரட்டை எண்ணிக்கையை கொண்ட மூலக்கூறுகள்
SeF4,
XeO2F2 ‒ Sp3d இனக்கலப்பு,
T‒வடிவம் மைய அணுவின் மீது ஒரு தனித்த எலக்ட்ரான் இரட்டை உள்ளது.
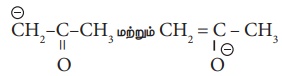 ஆகியவை
ஆகியவை
22.4 L கனஅளவு கொண்ட இரு கொள்கலன்கள் A மற்றும் B யில் முறையே 8g O2 மற்றும் 8g SO2 வாயுக்கள் STP நிலையில் நிரட்டப்பட்டுள்ளது. எனில்
ஆக்ஸிஜனின் மோல்களின் எண்ணிக்கை = 8g/32g
= 0.25 மோல்கள்
சல்பர்
டை
ஆக்ஸைடின் மோல்களின் எண்ணிக்கை = 8g/ 64g
= 0.125 மோல்கள்
மூலக்கூறுகளின் எண்ணிக்கைகளுக்கு இடையேயான விகிதம் = 0.25 : 0.125 = 2 : 1
3dxy
ஆர்பிட்டாலில் yz தளத்தில் எலக்ட்ரான் அடர்த்தி
பின்வரும் எம்மூலக்கூறுகளில் அனைத்து அணுக்களும் சமதளத்தில் உள்ளன.