Chemistry Tamil Medium - Online Test
கூற்று: கண்டுபிடிக்கப்பட்டுள்ள அனைத்து தனிமங்களுள் ஹீலியம் அதிக அயனியாக்கும் ஆற்றல் மதிப்பினை பெற்றுள்ளது.
காரணம்: கண்டுபிடிக்கப்பட்டுள்ள அனைத்து தனிமங்களுள் ஹீலியம் அதிக எலக்ட்ரான் நாட்ட மதிப்பினை பெற்றுள்ளது.
ஒரு மோல் அமிலம் கலந்த KMnO4 யை நிறமிழக்கச் செய்யத் தேவைப்படும் H2O2ன் மோல்களின் எண்ணிக்கை.
கூற்று: மோனோ ஹேலோ அரீன்களில், எலக்ட்ரான் கவர்பொருள் பதிலீட்டு வினை o‒ மற்றும் p‒ இடங்களில் நிகழ்கிறது.
காரணம்: ஹாலஜன் அணுவானது வளைய கிளர்வு நீக்கி
கூற்று : பொதுவாக கார மற்றும் காரமண் உலோகங்கள் சூப்பர் ஆக்சைடுகளை உருவாக்குகின்றன.
காரணம் : சூப்பர் ஆக்சைடுகளில் O மற்றும் O அணுக்களுக்கிடையே ஒற்றை பிணைப்பு உள்ளது.
கார
மற்றும் காரமண்
உலோகங்களில், K, Rb மற்றும் Cs ஆகியன
மட்டுமே சூப்பர் ஆக்ஸைடுகளை உருவாக்குகின்றன. சூப்பர் ஆக்ஸைடில் O2− ஆனது 3 எலக்ட்ரான் பிணைப்பினைக் கொண்டுள்ளது.
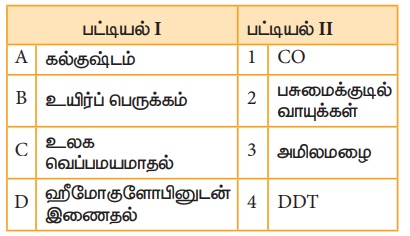
குறியீடு:
400K ல் 71.0 barல் CO2ன் அமுக்கதிறன் காரணி 0.8697 இந்த நிலையில் CO2ன் மோலார் கனஅளவு
அமுக்கத்திறன் காரணி
(z) = PV/nRT
V = (Z × nRT)/p
V = (0.8697 × 1 × 8.314 × 10−2 × 400) / 71bar = 0.41 dm3
ஒரு அமைப்பின் மீது 4kJ அளவு வேலை செய்யப்படுகிறது, மேலும் 1 kJ அளவு வெப்பமானது அமைப்பினால் வெளியேற்றப்படுகிறது எனில், அக ஆற்றலில் ஏற்படும் மாற்றம்
∆U = q + w
∆U = − 1kJ + 4kJ
∆U = +3kJ
X ⇌ Y + Z மற்றும் A ⇌ 2B ஆகிய வினைகளில் Kp1 மற்றும் K p2 ன் மதிப்புகள் 9:1 என்ற விகிதத்தில் உள்ளது. X மற்றும் A ன் பிரிகை வீதம் மற்றும் தொடக்கச் செறிவுகள் ஆகியன சமமாக இருந்தால், சமநிலையில் மொத்தம் அழுத்தம் P1 மற்றும் P2 வின் விகிதம் ‒‒‒‒‒‒‒‒‒‒‒

ஒரே வெப்பநிலையில், பின்வரும் கரைசல்களுள் எந்த இணை ஐசோடானிக் இணையாகும்?
Ba(NO3)2 , Na2
SO4 ன்
செறிவு
= 0.1 M
Ba(NO3)2 → Ba2+
+ 2NO‒3 ⇒ அயனிகள்
Na2 SO4 → 2Na+
+ SO2‒4 ⇒ அயனிகள்
செறிவு
மற்றும் அயனிகளின் எண்ணிக்கையை சமமாக
பெற்றுள்ள கரைசல்களின் சவ்வூடு பரவல்
அழுத்தம் சமமாகும்.
சம
சவ்வூடு பரவல்
அழுத்தத்தை பெற்றுள்ள கரைசல்கள் ஐசோடோனிக் கரைசல்களாகும்.
0.1 × 3 ion [Ba2+, 2NO3–]
0.1 × 3 ion [2 Na+, SO4–]
O22‒
டையா காந்த தன்மையுடையது கூடுதல் இரண்டு எலக்ட்ரான்கள் π*2Py
மற்றும் π*2Px எதிர் பிணைப்பு மூலக்கூறு ஆர்பிட்டாலில் இரட்டையாகின்றன