அத்தியாயம் 8 : அயனிச் சமநிலை - Online Test
Ag2C2O4
⇌
2Ag+ + C2O42–
[Ag+] = 2.24 × 10–4
mol L –1
[C2O42– ]
= (2.24 × 10–4 ) / (2) mol L –1
= 1.12 × 10–4 mol L –1
K sp = [Ag+]2
[C2O42– ]
(2.24 × 10–4 mol L–1)2
(1.12 × 10–4 mol L–1)
= 5.619 × 10–12 mol3
L–3
வெவ்வேறு செறிவுகளைக் கொண்ட NaOH மற்றும் HCl கரைசல்களை, வெவ்வேறு கன அளவுகளில் கலந்து பின் வரும் கரைசல்கள் தயாரிக்கப்பட்டன.

அவற்றில் எந்த கரைசலின் pH மதிப்பு 1 ஆக இருக்கும்?
HClன் மோல்களின் எண்ணிக்கை = 0.2 × 75 × 10–3 =15 ×
10–3
NaOHன் மோல்களின் எண்ணிக்கை = 0.2 × 25 × 10–3 = 5 ×
10–3
கலந்த பின் HCLன் மோல்களின் எண்ணிக்கை = 15 × 10–3 – 5 × 10–3
= 10 × 10–3
ஃHClன் செறிவு = HCl மோல்களின் எண்ணிக்கை / கனஅளவு (lit)
= ( 10×10–3 / 100×10–3
) = 0.1M
0.1 M HCl கரைசலின் pH = –log100.1 =1
298K ல், நீரில் BaSO4 இன் கரைதிறன் 2.42 × 10–3 gL–1
எனில் அதன் கரைதிறன் பெருக்க (Ksp) மதிப்பு
(BasO4 இன் மோலார் நிறை = 233g mol–1)
BaSO4 ⇌ Ba2+ + SO42–
ksp = (s) (s)
ksp = (s)2
= (2.42 × 10–3 g L–1)2
= (2.42 × 10–3 g L–1)2
/ (233g mol–1)
= (0.01038 ×10–3)2
= (1.038 × 10–5)2
= 1.077 × 10–10
= 1.08 × 10–10 mol2
L–2
தெவிட்டிய Ca(OH)2 கரைசலின் pH மதிப்பு 9 எனில், Ca(OH)2 இன் கரைதிறன் பெருக்க (Ksp) மதிப்பு
Ca(OH)2 ⇌ Ca2+ + 2OH–
PH = 9 என கொடுக்கப்பட்டது.
pOH = 14 – 9 = 5
(pOH = –log10[OH–])
ஃ [OH–] = 10– pOH
[OH–] = 10–5M
Ksp= [Ca2+]
[OH–]2
= (10–5 / 2 ) × (10–5)
⇒
0.5 ×
10–15
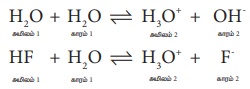
காரத்தாங்கல் கரைசல் வலிமை குறைகாரம் மற்றும் அதன் உப்பினைக் கொண்டுள்ளது.

BF3 → எலக்ட்ரான் குறை → லூயிஸ் அமிலம்
PF3 → எலக்ட்ரான் மிகுதி → லூயிஸ் காரம்
CF4 → நடுநிலை
→ லூயிஸ் அமிலம் காரம் இரண்டும் அல்ல
SiF4 → நடுநிலை → லூயிஸ் அமிலம் அல்ல லூயிஸ் காரமும் அல்ல
BF3 → எலக்ட்ரான் குறை → லூயிஸ் அமிலம்
PF3 → எலக்ட்ரான் மிகுதி → லூயிஸ் காரம்
CO → தனித்த எலக்ட்ரான் இரட்டைகள் → லூயிஸ் காரம்
F → இணையாத எலக்ட்ரான் இணைகள் → லூயிஸ் காரம்
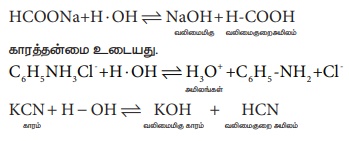
0.10M செறிவுடைய நீரிய பிரிடின் கரைசலில், பிரிடினியம் அயனியை (C5H5NH) உருவாக்கக் கூடிய பிரிடின் (C5H5N) மூலக்கூறு களின் சதவீதம் (Kb for C5H5N
= 1.7 × 10–9)