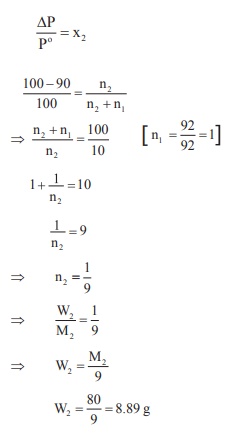அலகு 9 : கரைசல்கள் - Online Test
A மற்றும் B எனும் இரண்டு வாயுக்களின் ஹென்றி விதி மாறிலி மதிப்புகள் முறையே x மற்றும் y. A உடனான B யின் மோல் பின்ன விகிதம் 0.2. நீரில் கரையும் B மற்றும் A யின் மோல் பின்ன விகிதம்
கொடுக்கப்பட்டவை, (KH)A = x
(KH)B
= y
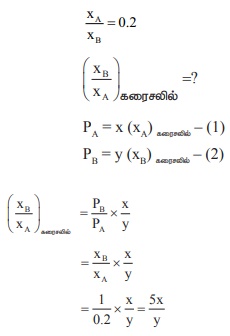
100°C வெப்பநிலையில், 100 கிராம் நீரில், 6.5 கிராம் கரைபொருள் கரைந்துள்ள கரைசலின் ஆவி அழுத்தம் 732mm Kb = 0.52, எனில், அந்த கரைசலின் கொதிநிலை மதிப்பு

Tb – 100 = 1.06
Tb = 100 + 1.06
= 101.06 ≈ 101oC
ரௌல்ட் விதிப்படி, ஒரு கரைசலின் ஒப்பு ஆவிஅழுத்தக்குறைவானது ______ க்கு சமம்
ஒரே வெப்பநிலையில், பின்வரும் கரைசல்களுள் எந்த இணை ஐசோடானிக் இணையாகும்?
Ba(NO3)2 , Na2
SO4 ன்
செறிவு
= 0.1 M
Ba(NO3)2 → Ba2+
+ 2NO‒3 ⇒ அயனிகள்
Na2 SO4 → 2Na+
+ SO2‒4 ⇒ அயனிகள்
செறிவு
மற்றும் அயனிகளின் எண்ணிக்கையை சமமாக
பெற்றுள்ள கரைசல்களின் சவ்வூடு பரவல்
அழுத்தம் சமமாகும்.
சம
சவ்வூடு பரவல்
அழுத்தத்தை பெற்றுள்ள கரைசல்கள் ஐசோடோனிக் கரைசல்களாகும்.
0.1 × 3 ion [Ba2+, 2NO3–]
0.1 × 3 ion [2 Na+, SO4–]
ஒரு மின்பகுளியில்லா சேர்மம் (X) இன் எளிய விகித வாய்ப்பாடு CH2O. 0.025M குளுக்கோஸ் கரைசல் பெற்றுள்ள சவ்வூடு பரவல் அழுத்தத்தை, அதே வெப்பநிலையில் 6 கிராம் X ஐ கொண்டுள்ள கரைசலும் பெற்றுள்ளது. X ன் மூலக்கூறு வாய்ப்பாடு
1 = மின்பகுளியல்லா சேர்மம்
2 = குளுக்கோஸ்
π1 அயனியாதல்= π2 குளுக்கோஸ்
C1 RT = C2 RT
C1 = C2
n1/V = n2/V
n1 = n2
W1 / M1 = W2
/ M2
மூலக்கூறு நிறை
= n எளிய விகித
வாய்ப்பாடு நிறை
W1 = 6 கி
M1 = n × 30; CH2O
12 + 2 + 16 = 30
n2 = 0.025
ஃ
6/n × 30 = 0.025
ஃ
n = 6 / 0.025 × 30 = 8
மூலக்கூறு வாய்ப்பாடு = n × எளிய விகித
வாய்ப்பாடு
= 8 × (CH2O) = C8H16O8
கொடுக்கப்பட்ட வெப்பநிலையில், நீரில் ஆக்ஸிஜன் கரைந்த கரைசலின் KH
மதிப்பு 4×104 atm. காற்றில் ஆக்ஸிஜனின் பகுதி அழுத்தம் 0.4 atm, எனில், கரைசலில் ஆக்ஸிஜனின் மோல் பின்னம்
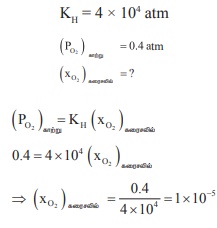
1.25M கந்தக அமிலத்தின் நார்மாலிட்டி
H2SO4 நார்மாலிட்டி = (இடம்பெயரும் H+ அயனிகள்)×M
= 2 × 1.25
= 2.5 N
இரண்டு திரவங்கள் X மற்றும் Y ஆகியன கலக்கப்படும்போது வெதுவெதுப்பான கரைசலைத் தருகின்றன. அந்தக் கரைசலானது
நீரில் சர்க்கரைக் கரைசலின் ஒப்பு ஆவி அழுத்தக்குறைவு 3.5 × 10‒3. அந்த கரைசலில் நீரின் மோல் பின்னம்
ΔP / Po = Xசர்க்கரை
3.5 × 10‒3
= Xசர்க்கரை
Xசர்க்கரை + XH2O
= 1
ஃ
XH2O = 1 – 0.0035 = 0.9965
92 கிராம் டொலுயீனின், ஆவிஅழுத்தத்தை 90% க்கு குறைப்பதற்கு, அதில் கரைக்கத் தேவையான எளிதில் ஆவியாகாத கரைபொருளின் நிறை (மோலார் நிறை 80 g mol‒1)