அலகு 8 : இயற் மற்றும் வேதிச்சமநிலை - Online Test
ஒரு மீள் வினையின் Kp மற்றும் Kf மதிப்புகள் முறையே 0.8 × 10‒5 மற்றும் 1.6 × 10‒4 எனில், சமநிலை மாறிலியின் மதிப்பு ‒‒‒‒‒‒‒‒‒
1. Kp = 0.8 × 10‒5
; Kf = 1.6 × 10‒4; KC = ?
KC = Kf / Kp
= 1.6×10‒4 / 0.8×10‒5 = 20
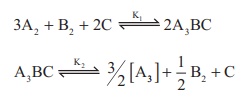
ஆகிய சமநிலைகளுக்கு ஒரு குறிப்பிட்ட வெப்பம் மற்றும் அழுத்த நிலையில் சமநிலை மாறிலிகளின் மதிப்புகள் கொடுக்கப்பட்டுள்ளன. K1 மற்றும் K2 விற்கு இடையேயான தொடர்பு யாது?
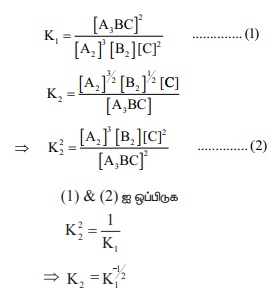
ஒரு வினையின் சமநிலை மாறிலி அறைவெப்பநிலையில் K1 மற்றும் 700K ல் K2 ஆகும். K1 > K2 எனில்,

வெப்பநிலை உயரும்போது K மதிப்பு குறைகிறது. எனவே
முன்னோக்கு வினை
வெப்பம் உமிழ்வினை.
N2
(g) மற்றும் H2 (g) ஆகியவற்றிலிருந்து NH3 உருவாதல் ஒரு மீள் வினையாகும்
N2
(g) + 3H2 (g) ⇌ 2NH3 (g) + வெப்பம் இவ்வினையின் மீது வெப்பநிலை உயர்வினால் ஏற்படும் விளைவு என்ன?
வெப்ப நிலை அதிகரிப்பு வெப்ப கொள்வினைக்கு சாதகமாக அமையும்.
அமோனியா உருவாதல் வெப்ப உமிழ் வினை என கொடுக்கப்பட்டுள்ளது
எனவே பின்னோக்கிய வினை வெப்்ப உமிழ் வினை.
வெப்பநிலை அதிகரிப்பு இடதுபுறம் நகர்த்தும்
முன்னோக்கு வினை
வெப்பம் உமிழ்வினை எனவே
வெப்பநிலை உயர்வு
பின்னோக்கு வினையை
தூண்டுகிறது.
குளிர்ந்த நீரில் கார்பன்டை ஆக்சைடு வாயுவின் கரைதிறனை எவ்வாறு அதிகரிக்கலாம்.
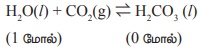
அழுத்த அதிகரிப்பு, முன்னோக்கு வினையை ஆதரிக்கும் .
ஒரு
நீர்மத்தில் வாயுவின் கரைதிறனானது அழுத்தத்தை அதிகரிக்கும் போது
அதிகரிக்கிறது.
கீழ் கண்டவற்றில் எது சரியான கூற்று அல்ல?
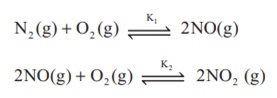
மேற்கண்டுள்ள வினைகளின் சமநிலை மாறிலிகளின் மதிப்புகள் முறையே K1
மற்றும் K2
NO2 (g) ⇌ ½ N2 (g) + O2 (g) என்ற வினையின் சமநிலை மாறிலி யாது?
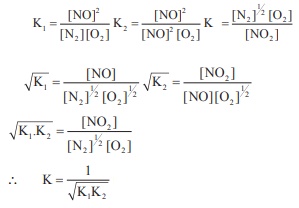
2A(g) ⇌ 2B(g) + C2(g)
என்ற சமநிலையில், 400K வெப்பநிலையில் A, B மற்றும் C2 வின் சமநிலைச்செறிவுகள் முறையே 1 × 10‒4 M. 2.0 × 10‒3 M, 1.5
× 10‒4 M. 400K, வெப்பநிலையில் சமநிலையின் KC மதிப்பு யாது?
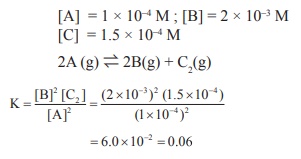
= 0.06 M
ஒரு வினைக்கு சமநிலை மாறிலி மதிப்பு 3.2 × 10‒6 என்பதன் பொருள் சமநிலையானது

KC = 10‒3 ‒ 10‒3
⇒ சமநிலை
KC >103 ⇒ முன்னோக்கு வினை
நடைபெறும், வினை
முற்றுபெறும்.
KC < 10‒3 ⇒ பின்னோக்கு வினை
நடைபெறும், வினை
முற்றுபெறாது.
N2(g)
+ 3H2 (g) ⇌ 2NH3 (g) என்ற வினையின் Kc / Kp = ?
N2(g) + 3H2 (g) ⇌ 2NH3 (g) என்ற வினைக்கு,
∆ng = 2 – 4 = ‒2
Kp = KC(RT) ∆ng
Kp = KC(RT)‒2
Kp = KC (1/
(RT)2)
Kp(RT)2 = KC
KC / Kp = (RT)2