Ó«ģÓ«▓Ó«ĢÓ»ü 5 : Ó«ĢÓ«ŠÓ«░ Ó««Ó«▒Ó»ŹÓ«▒Ó»üÓ««Ó»Ź Ó«ĢÓ«ŠÓ«░Ó««Ó«ŻÓ»Ź Ó«ēÓ«▓Ó»ŗÓ«ĢÓ«ÖÓ»ŹÓ«ĢÓ«│Ó»Ź - Online Test
Ó«ĢÓ«ŠÓ«░ Ó«ēÓ«▓Ó»ŗÓ«ĢÓ«ÖÓ»ŹÓ«ĢÓ«│Ó»üÓ«ĢÓ»ŹÓ«ĢÓ»ü, Ó«¬Ó«┐Ó«®Ó»ŹÓ«ĄÓ«░Ó»üÓ«ĄÓ«®Ó«ĄÓ«▒Ó»ŹÓ«▒Ó»üÓ«│Ó»Ź Ó«ÄÓ«©Ó»ŹÓ«ż Ó«ĄÓ«░Ó«┐Ó«ÜÓ»łÓ«¬Ó»ŹÓ«¬Ó«ŻÓ»ŹÓ«¬Ó»ü Ó«żÓ«ĄÓ«▒Ó«ŠÓ«®Ó«żÓ»ü?
Ó«¬Ó»ŖÓ«¤Ó»ŹÓ«¤Ó«ŠÓ«ÜÓ«┐Ó«»Ó««Ó«ŠÓ«®Ó«żÓ»ü Ó«ÜÓ»ŗÓ«¤Ó«┐Ó«»Ó«żÓ»ŹÓ«żÓ»ł Ó«ĄÓ«┐Ó«¤
Ó«ćÓ«▓Ó»ćÓ«ÜÓ«ŠÓ«®Ó«żÓ»ü.
(Ó«ģÓ«¤Ó»ŹÓ«¤Ó«ĄÓ«ŻÓ»ł 5.3 Ó«ÉÓ«¬Ó»Ź
Ó«¬Ó«ŠÓ«░Ó»ŹÓ«ĢÓ»ŹÓ«Ģ)
Ó«ģÓ«¤Ó«░Ó»ŹÓ«żÓ»ŹÓ«żÓ«┐Ó«»Ó«┐Ó«®Ó»Ź Ó«ÜÓ«░Ó«ŠÓ«ÜÓ«░Ó«┐
Ó«ĄÓ«░Ó«┐Ó«ÜÓ»ł
Li < K Na < Rb < Cs
0.54 < 0.86 < 0.97 < 1.53
< 1.90 (in g cmŌłÆ3)
Ó«¬Ó«┐Ó«®Ó»ŹÓ«ĄÓ«░Ó»üÓ«ĄÓ«®Ó«ĄÓ«▒Ó»ŹÓ«▒Ó»üÓ«│Ó»Ź Ó«żÓ«ĄÓ«▒Ó«ŠÓ«® Ó«ĢÓ»éÓ«▒Ó»ŹÓ«▒Ó»ü Ó«ÄÓ«żÓ»ü?
Ó«ĢÓ«ŠÓ«░
Ó«ēÓ«▓Ó»ŗÓ«Ģ
Ó«©Ó»ćÓ«░Ó»Ź
Ó«ģÓ«»Ó«®Ó«┐Ó«ĢÓ«│Ó»üÓ«│Ó»Ź Li+ Ó«ģÓ«»Ó«®Ó«┐Ó«»Ó«ŠÓ«®Ó«żÓ»ü Ó«ģÓ«żÓ«┐Ó«Ģ
Ó«©Ó»ĆÓ«░Ó»ćÓ«▒Ó»ŹÓ«▒Ó»ü Ó«żÓ«®Ó»ŹÓ««Ó»łÓ«»Ó»ł Ó«¬Ó»åÓ«▒Ó»ŹÓ«▒Ó»üÓ«│Ó»ŹÓ«│Ó«żÓ»ü.
Li+ > Na+ >
K+ > Rb+ > Cs+
Ó«¬Ó«┐Ó«®Ó»ŹÓ«ĄÓ«░Ó»üÓ««Ó»Ź Ó«ÜÓ»ćÓ«░Ó»ŹÓ««Ó«ÖÓ»ŹÓ«ĢÓ«│Ó«┐Ó«▓Ó»Ź Ó«ÄÓ«żÓ»ü Ó«ĢÓ«ŠÓ«░ Ó«ēÓ«▓Ó»ŗÓ«ĢÓ«ÖÓ»ŹÓ«ĢÓ«│Ó»üÓ«¤Ó«®Ó»Ź Ó«ĄÓ«┐Ó«®Ó»łÓ«¬Ó»ŹÓ«¬Ó«¤Ó»ŹÓ«¤Ó»ü H2 Ó«ĄÓ«ŠÓ«»Ó»üÓ«ĄÓ»ł Ó«ĄÓ»åÓ«│Ó«┐Ó«»Ó»ćÓ«▒Ó»ŹÓ«▒Ó»üÓ«ĄÓ«żÓ«┐Ó«▓Ó»ŹÓ«▓Ó»ł?
Ó«ĢÓ»ŖÓ«¤Ó»üÓ«ĢÓ»ŹÓ«ĢÓ«¬Ó»ŹÓ«¬Ó«¤Ó»ŹÓ«¤Ó»üÓ«│Ó»ŹÓ«│ Ó«ģÓ«®Ó»łÓ«żÓ»ŹÓ«żÓ»üÓ«ÜÓ»Ź Ó«ÜÓ»ćÓ«░Ó»ŹÓ««Ó«ÖÓ»ŹÓ«ĢÓ«│Ó»üÓ««Ó»Ź Ó«ĢÓ«ŠÓ«░
Ó«ēÓ«▓Ó»ŗÓ«ĢÓ«ÖÓ»ŹÓ«ĢÓ«│Ó»üÓ«¤Ó«®Ó»Ź Ó«ĄÓ«┐Ó«®Ó»łÓ«¬Ó»ŹÓ«¬Ó«¤Ó»ŹÓ«¤Ó»ü Ó«╣Ó»łÓ«¤Ó»ŹÓ«░Ó«£Ó«®Ó»Ź Ó«ĄÓ«ŠÓ«»Ó»üÓ«ĄÓ»ł
Ó«ĄÓ»åÓ«│Ó«┐Ó«»Ó»ćÓ«▒Ó»ŹÓ«▒Ó»üÓ«ĢÓ«┐Ó«®Ó»ŹÓ«▒Ó«®. Ó«ÄÓ«®Ó«ĄÓ»ć
Ó«ćÓ«ĄÓ«▒Ó»ŹÓ«▒Ó«┐Ó«▓Ó»Ź Ó«ÅÓ«żÓ»üÓ««Ó«┐Ó«▓Ó»ŹÓ«▓Ó»ł Ó«ÄÓ«®Ó»ŹÓ«¬Ó«żÓ»ć
Ó«ÜÓ«░Ó«┐Ó«»Ó«ŠÓ«®
Ó«ĄÓ«┐Ó«¤Ó»łÓ«»Ó«ŠÓ«ĢÓ»üÓ««Ó»Ź.
Ó«ĢÓ»ĆÓ«┤Ó»ŹÓ«ĢÓ»ŹÓ«ĢÓ«ŻÓ»ŹÓ«¤ Ó«ĄÓ«┐Ó«®Ó»ł Ó«©Ó«┐Ó«ĢÓ«┤Ó»ŹÓ«ĄÓ«żÓ«▒Ó»ŹÓ«ĢÓ»ü Ó«¬Ó«┐Ó«®Ó»ŹÓ«ĄÓ«░Ó»üÓ«ĄÓ«®Ó«ĄÓ«▒Ó»ŹÓ«▒Ó»üÓ«│Ó»Ź Ó«ÄÓ«żÓ»ü Ó««Ó«┐Ó«Ģ Ó«ģÓ«żÓ«┐Ó«Ģ Ó«ćÓ«»Ó«▓Ó»ŹÓ«¬Ó«┐Ó«®Ó»łÓ«ĢÓ»Ź (tendency) Ó«ĢÓ»ŖÓ«ŻÓ»ŹÓ«¤Ó»üÓ«│Ó»ŹÓ«│Ó«żÓ»ü.

Li+ Ó«®Ó»Ź Ó«©Ó»ĆÓ«░Ó»ćÓ«▒Ó»ŹÓ«▒ Ó«åÓ«▒Ó»ŹÓ«▒Ó«▓Ó»Ź
Ó«ģÓ«żÓ«┐Ó«ĢÓ««Ó»Ź.
Ó«ÄÓ«®Ó«ĄÓ»ć
Li+ Ó«åÓ«®Ó«żÓ»ü
Ó«©Ó»ĆÓ«░Ó»Ź
Ó«ŖÓ«¤Ó«ĢÓ«żÓ»ŹÓ«żÓ«┐Ó«▓Ó»Ź Ó«©Ó«┐Ó«▓Ó»łÓ«¬Ó»ŹÓ«¬Ó»üÓ«żÓ»Ź Ó«żÓ«®Ó»ŹÓ««Ó»ł
Ó«ģÓ«¤Ó»łÓ«ĢÓ«┐Ó«▒Ó«żÓ»ü.
Ó«ÜÓ»ŗÓ«¤Ó«┐Ó«»Ó««Ó»Ź Ó«ÄÓ«żÓ«┐Ó«▓Ó»Ź Ó«ÜÓ»ćÓ««Ó«┐Ó«ĢÓ»ŹÓ«ĢÓ«¬Ó»ŹÓ«¬Ó«¤Ó»üÓ«ĢÓ«┐Ó«▒Ó«żÓ»ü?
RbO2
Ó«ÜÓ»ćÓ«░Ó»ŹÓ««Ó««Ó»Ź Ó«ÆÓ«░Ó»ü
RbO2 Ó«åÓ«®Ó«żÓ»ü Ó«ÆÓ«░Ó»ü Ó«ÜÓ»éÓ«¬Ó»ŹÓ«¬Ó«░Ó»Ź Ó«åÓ«ĢÓ»ŹÓ«ĖÓ»łÓ«¤Ó»ü Ó«åÓ«ĢÓ»üÓ««Ó»Ź.
Ó«ćÓ«żÓ»ü
Rb+ Ó««Ó«▒Ó»ŹÓ«▒Ó»üÓ««Ó»Ź O2ŌłÆ Ó«ģÓ«»Ó«®Ó«┐Ó«ĢÓ«│Ó»łÓ«ĢÓ»Ź Ó«ĢÓ»ŖÓ«ŻÓ»ŹÓ«¤Ó»üÓ«│Ó»ŹÓ«│Ó«żÓ»ü. Ó««Ó»ćÓ«▓Ó»üÓ««Ó»Ź
O2ŌłÆ Ó«ģÓ«»Ó«®Ó«┐Ó«»Ó«ŠÓ«®Ó«żÓ»ü Ó«ÆÓ«░Ó»ü
Ó«żÓ«®Ó«┐Ó«żÓ»ŹÓ«ż
Ó«ÄÓ«▓Ó«ĢÓ»ŹÓ«¤Ó»ŹÓ«░Ó«ŠÓ«®Ó»łÓ«ĢÓ»Ź Ó«ĢÓ»ŖÓ«ŻÓ»ŹÓ«¤Ó»üÓ«│Ó»ŹÓ«│Ó«żÓ»ü. Ó«ÄÓ«®Ó«ĄÓ»ć
Ó«ćÓ«żÓ»ü
Ó«¬Ó«ŠÓ«░Ó«Š
Ó«ĢÓ«ŠÓ«©Ó»ŹÓ«żÓ«żÓ»Ź Ó«żÓ«®Ó»ŹÓ««Ó»łÓ«»Ó»üÓ«¤Ó»łÓ«»Ó«żÓ»ü.
Ó«żÓ«ĄÓ«▒Ó«ŠÓ«® Ó«ĢÓ»éÓ«▒Ó»ŹÓ«▒Ó»łÓ«ĢÓ»Ź Ó«ĢÓ«ŻÓ»ŹÓ«¤Ó«▒Ó«┐Ó«»Ó«ĄÓ»üÓ««Ó»Ź.
Ó«ÜÓ«ŠÓ«▓Ó»ŹÓ«ĄÓ»ć
Ó««Ó»üÓ«▒Ó»łÓ«»Ó«┐Ó«▓Ó»Ź Ó«¬Ó»ŖÓ«¤Ó»ŹÓ«¤Ó«ŠÓ«ÜÓ«┐Ó«»Ó««Ó»Ź Ó«ĢÓ«ŠÓ«░Ó»ŹÓ«¬Ó«®Ó»ćÓ«¤Ó»ŹÓ«¤Ó»ł Ó«żÓ«»Ó«ŠÓ«░Ó«┐Ó«ĢÓ»ŹÓ«Ģ Ó«ćÓ«»Ó«▓Ó«ŠÓ«żÓ»ü.
Ó«¬Ó»ŖÓ«¤Ó»ŹÓ«¤Ó«ŠÓ«ÜÓ«┐Ó«»Ó««Ó»Ź Ó«¬Ó»ł
Ó«ĢÓ«ŠÓ«░Ó»ŹÓ«¬Ó«®Ó»ćÓ«¤Ó»Ź Ó«©Ó»ĆÓ«░Ó«┐Ó«▓Ó»Ź
Ó«ĢÓ»üÓ«▒Ó«┐Ó«¬Ó»ŹÓ«¬Ó«┐Ó«¤Ó«żÓ»ŹÓ«żÓ«ĢÓ»ŹÓ«Ģ Ó«ģÓ«│Ó«ĄÓ«┐Ó«▓Ó»Ź
Ó«ĢÓ«░Ó»łÓ«»Ó«ĢÓ»Ź
Ó«ĢÓ»éÓ«¤Ó«┐Ó«»Ó«żÓ»ü. Ó«ÄÓ«®Ó«ĄÓ»ć
Ó«ĄÓ»ĆÓ«┤Ó»ŹÓ«¬Ó»ŹÓ«¬Ó«¤Ó«┐Ó«ĄÓ«ŠÓ«ĄÓ«żÓ«┐Ó«▓Ó»ŹÓ«▓Ó»ł.
Ó«▓Ó«┐Ó«żÓ»ŹÓ«żÓ«┐Ó«»Ó««Ó»Ź Ó«ÄÓ«żÓ«®Ó»üÓ«¤Ó«®Ó»Ź Ó««Ó»éÓ«▓Ó»łÓ«ĄÓ«┐Ó«¤Ó»ŹÓ«¤ Ó«żÓ»ŖÓ«¤Ó«░Ó»ŹÓ«¬Ó»ü Ó«ēÓ«¤Ó»łÓ«»Ó«żÓ»ü?
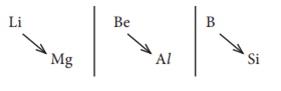
Ó«ĢÓ«ŠÓ«░ Ó«ēÓ«▓Ó»ŗÓ«Ģ Ó«╣Ó»ćÓ«▓Ó»łÓ«¤Ó»üÓ«ĢÓ«│Ó«┐Ó«®Ó»Ź, Ó«ģÓ«»Ó«®Ó«┐Ó«żÓ»Ź Ó«żÓ«®Ó»ŹÓ««Ó»łÓ«»Ó«┐Ó«®Ó»Ź Ó«ÅÓ«▒Ó»üÓ«ĄÓ«░Ó«┐Ó«ÜÓ»ł
Ó«ģÓ«»Ó«®Ó«┐Ó«¬Ó»Ź
Ó«¬Ó«ŻÓ»ŹÓ«¬Ó»ü
(Ó«ÄÓ«▓Ó«ĢÓ»ŹÓ«¤Ó»ŹÓ«░Ó«ŠÓ«®Ó»Ź Ó«ĢÓ«ĄÓ«░Ó»ŹÓ«żÓ«®Ó»ŹÓ««Ó»łÓ«»Ó«┐Ó«▓Ó»Ź Ó«ĄÓ»ćÓ«▒Ó»üÓ«¬Ó«ŠÓ«¤Ó»ü)
MI < M Br < MCl < MF
Ó«ÄÓ««Ó»ŹÓ««Ó»üÓ«▒Ó»łÓ«»Ó«┐Ó«▓Ó»Ź, Ó«ēÓ«░Ó»üÓ«ĢÓ«┐Ó«» Ó«ÜÓ»ŗÓ«¤Ó«┐Ó«»Ó««Ó»Ź Ó«╣Ó»łÓ«¤Ó»ŹÓ«░Ó«ŠÓ«ĢÓ»ŹÓ«ÜÓ»łÓ«¤Ó»ü Ó««Ó«┐Ó«®Ó»ŹÓ«®Ó«ŠÓ«▒Ó»ŹÓ«¬Ó«ĢÓ»üÓ«ĢÓ»ŹÓ«ĢÓ«¬Ó»ŹÓ«¬Ó«¤Ó»ŹÓ«¤Ó»ü, Ó«ÜÓ»ŗÓ«¤Ó«┐Ó«»Ó««Ó»Ź Ó«¬Ó«┐Ó«░Ó«┐Ó«żÓ»ŹÓ«żÓ»åÓ«¤Ó»üÓ«ĢÓ»ŹÓ«ĢÓ«¬Ó»ŹÓ«¬Ó«¤Ó»üÓ«ĢÓ«┐Ó«▒Ó«żÓ»ü?
Ó«ĢÓ«ŠÓ«ĖÓ»ŹÓ«¤Ó»ŹÓ«®Ó«░Ó»Ź Ó««Ó»üÓ«▒Ó»ł
NaOH Ōćī Na+ + OHŌłÆ
Ó«ÄÓ«żÓ«┐Ó«░Ó»ŹÓ««Ó«┐Ó«®Ó»ŹÓ«ĄÓ«ŠÓ«»Ó»Ź: Na+ + eŌłÆ ŌåÆ Na
Ó«©Ó»ćÓ«░Ó»ŹÓ««Ó«┐Ó«®Ó»ŹÓ«ĄÓ«ŠÓ«»Ó»Ź : 2OH ŌåÆ H2O + ┬Į O2 + eŌłÆ