அத்தியாயம் 9 : மின் வேதியியல் - Online Test
கீழே கொடுக்கப்பட்டுள்ள படத்தில் காட்டியுள்ள வாறு வெவ்வேறு emf மதிப்புகளைச் சார்ந்து புரோமினின் ஆக்ஸிஜனேற்ற நிலைகளில் ஏற்படும் மாற்றத்தை கருத்திற் கொள்க.
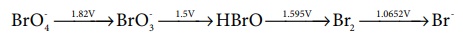
இவற்றில் விகிதச் சிதைவு அடையும் கூறு எது?
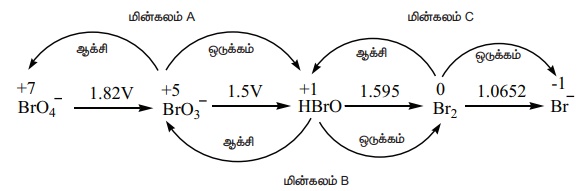
(Eமின்கலம்) A = –1.82 + 1.5=–0.32 V
(Eமின்கலம்) B = –1.5+ 1.595 = +
0.095 V
(Eமின்கலம்) C = –1.595 + 1.0652 = –
0.529 V
ஃவிகிதச் சிதைவடைவது HBrO.
பின்வரும் கலவினைக்கு 2Fe3+(aq) + 21–(aq) → 2Fe2+(aq) + I2(aq) 298K வெப்பநிலையில் E° கலம் = 0.24V எனில், கலவினையின் திட்ட கட்டிலா ஆற்றல் மாற்ற (∆G°) மதிப்பு
n= 2; E°cell = 0.24V; ∆G° = ?; F= 96500C
∆G° = – nFE°
∆G° = –2 x 96500 × 0.24
∆G° = – 46320 J mol–1
∆G° = – 46.32 KJ mol–1
ஒரு குறிப்பிட்ட அளவு மின்னோட்டமானது 2 மணி நேரத்தில் 0.504 கிராம் ஹைட்ரஜனை விடுவிக்கிறது. அதே அளவு மின்னோட்டத்தை அதே அளவு நேரத்திற்கு காப்பர் சல்பேட் கரைசலின் வழியே செலுத்தினால் எவ்வளவு கிராம் காப்பர் வீழ்படிவாக்கப்படும்?
m1 = 0.504g
m2 = ?
e1 = 1.008
e2 = 31.77
m1 / m2 = e1
/ e2
m2 = [ m1 × e2 ]
/ e1 = (0.504×31.77)
/ 1.008
= 15.885 g
25°C வெப்பநிலையில் 1MY– மற்றும் 1MZ– ஆகியவற்றை
கொண்டுள்ள கரைசலின் வழியே 1 atm அழுத்தத்தில் X எனும் வாயு குமிழிகளாக செலுத்தப்படுகிறது. அவற்றின் ஒடுக்க
மின்னழுத்தங்கள் Z > Y > X எனில்,

Z ஆனது Y மற்றும் X ஐ ஆக்சிஜனேற்றமடையச் செய்கிறது
Y ஆனது X ஐ ஆக்சிஜனேற்றமடையச் செய்கிறது Zஐ ஒடுக்கமடையச் செய்கிறது
X ஆனது Y மற்றும் Z ஐ ஒடுக்கமடையச் செய்கிறது
கலவினை : A + 2B+ → A2+ + 2B;
A2+ + 2e– → A E° = + 0.34 V மற்றும்
300K வெப்பநிலையில் இந்தகலவினைக்கு log10K = 15.6 at 300K எனில் B+ + e– → B எனும் கலவினைக்கு E° மதிப்பை காண்க
A + 2B+ + A2+ → 2B
E°cell =?
அரைமின்கலவினை :
நேர்மின்வாய் A→ A2+ + 2e–
E°ox =–0.34V [Given : A2+
+ 2e–→ A
E°=+0.34V]
எதிர்மின்வாய் 2B+ + 2e– → 2B Eored =?
log10 K = 15.6; T= 300K;
n = 2;
R = 8.314 JK–1 mol–1
∆G° =–nFE°
∆G° =–2.303 RT log K
ஃ – nFEo = – 2.303 RT log K
ஃ Eocell = –2.303 RT logK / nF
ஃ Eocell = [ –2.303 × 8.314 × 300 ×
15.6 ] / [2 × 96500]
ஃ Eocell = 0.4643 V
Eocell = Eooxid
+ Eored
ஃ Eored
= Eocell – Eooxid
= 0.4643 – (–0.34)
= 0.4643 + 0.34
Eored = 0.8043
V = 0. 80 V